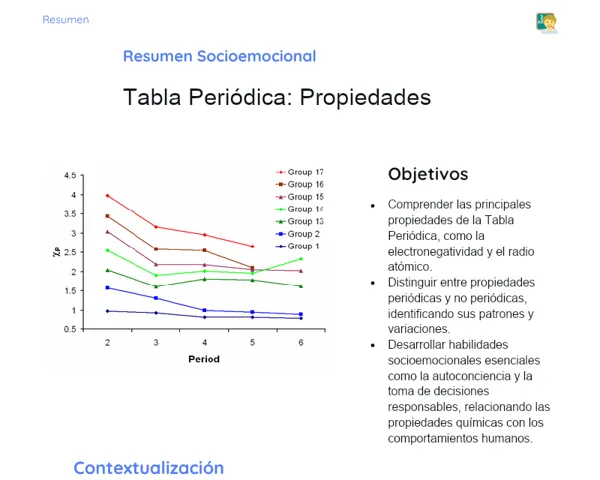
Objetivos
1. 🔍 Identificar y diferenciar las principales fuerzas intermoleculares: fuerzas de London, fuerzas dipolo-dipolo y enlaces de hidrógeno.
2. 🌍 Aplicar lo aprendido para analizar y predecir el comportamiento de diferentes sustancias según sus fuerzas intermoleculares predominantes.
3. 🏆 Desarrollar habilidades de argumentación y justificación al explicar y defender elecciones relacionadas con las fuerzas intermoleculares en escenarios prácticos o experimentales.
Contextualización
¿Sabías que los enlaces intermoleculares no son solo conceptos abstractos de la química, sino fuerzas invisibles que influyen en muchos aspectos de nuestra vida cotidiana? Por ejemplo, la capacidad del agua para formar una 'piel' en su superficie, conocida como tensión superficial, es fundamental para muchos procesos biológicos y climáticos. Comprender estas fuerzas puede ayudar en todo, desde la cocina, donde la elección de ingredientes y métodos de preparación depende de sus interacciones moleculares, hasta tecnologías innovadoras que utilizan materiales con propiedades específicas basadas en estos enlaces.
Temas Importantes
Fuerzas de London
Las fuerzas de London, también conocidas como fuerzas de dispersión de London, son interacciones intermoleculares que se presentan en todas las sustancias, sin importar su polaridad. Surgen de fluctuaciones temporales en la distribución electrónica que pueden generar dipolos instantáneos. Cuanto mayor es la masa molar de la sustancia, mayor es la polarizabilidad y, por lo tanto, la fuerza de las fuerzas de London.
-
Se encuentran en todas las sustancias, pero son predominantes en sustancias no polares o débilmente polares.
-
Facilitan la adhesión de moléculas en materiales como plásticos y gases nobles.
-
Son importantes para entender propiedades como los puntos de ebullición y fusión en moléculas no polares.
Fuerzas Dipolo-Dipolo
Las fuerzas dipolo-dipolo son interacciones que ocurren entre moléculas polarizadas, donde el extremo positivo de una molécula atrae el extremo negativo de otra. Estas fuerzas son más fuertes que las fuerzas de London y son cruciales para explicar la miscibilidad de sustancias con diferentes polaridades, como el agua y el etanol.
-
Están presentes en sustancias polarizadas, como compuestos moleculares con diferencias significativas en las electronegatividades de los átomos.
-
Son determinantes para la formación de estructuras más organizadas en sólidos y líquidos.
-
Influyen en propiedades como el punto de ebullición y la solubilidad.
Enlace de Hidrógeno
El enlace de hidrógeno es un tipo especial de fuerza dipolo-dipolo que se forma específicamente entre el hidrógeno, unido a átomos altamente electronegativos (como F, O o N), y un átomo de estos elementos en otra molécula. Es la fuerza intermolecular más fuerte y juega un papel fundamental en muchos fenómenos biológicos y químicos, como la estructura del ADN y la estabilidad de proteínas.
-
Mucho más fuerte que las fuerzas de London y las fuerzas dipolo-dipolo, influenciando drásticamente las propiedades de las sustancias.
-
Fundamental para entender la alta solubilidad del agua y su capacidad para formar enlaces de hidrógeno con otras moléculas.
-
Esencial para comprender procesos biológicos y farmacéuticos, donde las interacciones moleculares son clave.
Términos Clave
-
Fuerzas de London: Fuerzas intermoleculares que actúan en todas las sustancias, resultantes de fluctuaciones temporales en la distribución electrónica.
-
Dipolo-Dipolo: Un tipo de fuerza intermolecular que ocurre entre moléculas polarizadas, donde el extremo positivo de una molécula atrae el extremo negativo de otra.
-
Enlace de Hidrógeno: Una forma especial de interacción dipolo-dipolo que se da entre el hidrógeno unido a átomos altamente electronegativos y un átomo correspondiente en otra molécula.
Para Reflexionar
-
¿Cómo puede entender los enlaces intermoleculares ayudar a resolver problemas de solubilidad en productos farmacéuticos o químicos?
-
¿De qué manera influyen las fuerzas intermoleculares en la selección de materiales para la fabricación de equipos electrónicos?
-
¿Cuál es el impacto de los enlaces intermoleculares en el desarrollo de nuevos materiales para aplicaciones tecnológicas y medioambientales?
Conclusiones Importantes
-
Revisamos las principales fuerzas intermoleculares: fuerzas de London, fuerzas dipolo-dipolo y enlaces de hidrógeno, y cómo influyen en propiedades como el punto de ebullición, la solubilidad y la tensión superficial.
-
Discutimos aplicaciones prácticas de estas fuerzas, como en la cocina y la industria farmacéutica, ilustrando su importancia en la vida cotidiana y en los procesos industriales.
-
Exploramos cómo comprender los enlaces intermoleculares es crucial para los avances en campos como la biología, la química y la ciencia de materiales, abriendo puertas a innovaciones tecnológicas y científicas.
Para Ejercitar el Conocimiento
- Simulación Digital de Moléculas: Utiliza software de simulación molecular para visualizar y manipular moléculas, observando cómo las diferentes fuerzas intermoleculares influyen en su estructura y comportamiento. 2. Experimento de Miscibilidad: Crea un pequeño laboratorio en casa y prueba la miscibilidad de diferentes sustancias (como agua, aceite y alcohol) para observar directamente las fuerzas intermoleculares en acción. 3. Discusión Basada en Artículo Científico: Lee un artículo reciente que aplique el concepto de enlaces intermoleculares en un contexto práctico (por ejemplo, el desarrollo de nuevos materiales) y presenta un resumen y tus ideas en un foro en línea para la clase.
Desafío
Crea una infografía digital que explique las tres principales fuerzas intermoleculares, destacando ejemplos de sustancias cotidianas donde cada una predomina. Comparte tu infografía en un tablero de clase virtual para que todos puedan aprender de los diferentes enfoques.
Consejos de Estudio
-
Usa mapas mentales para conectar las diferentes fuerzas intermoleculares con sus propiedades y aplicaciones, ayudando a visualizar y memorizar el contenido.
-
Mira videos educativos que demuestren experimentos prácticos sobre enlaces intermoleculares para complementar tu aprendizaje teórico.
-
Participa en foros en línea o grupos de estudio para discutir preguntas y aplicaciones prácticas de los enlaces intermoleculares con tus compañeros.