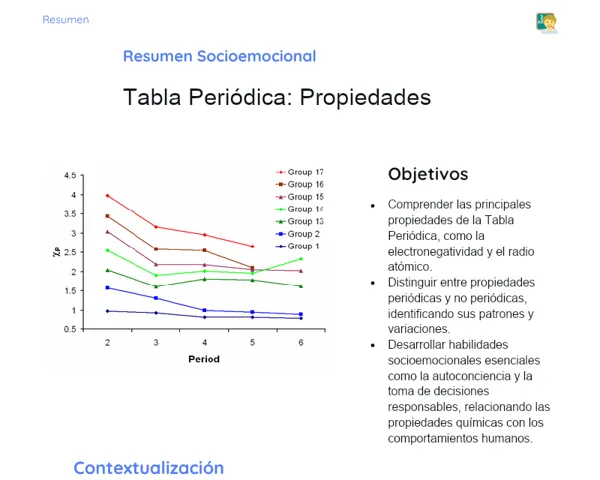
Objetivos
1. 🇦🇷 Comprender claramente la diferencia entre disociación e ionización, y ser capaz de identificar cada proceso en diversas situaciones.
2. 🇦🇷 Desarrollar habilidades tanto prácticas como teóricas para analizar soluciones químicas y predecir su comportamiento en el agua.
Contextualización
¿Sabías que la forma en que los medicamentos se disuelven en el cuerpo puede depender de si la sustancia pasa por disociación o ionización? Este concepto no solo es fundamental para los científicos que buscan formular medicamentos más efectivos, sino que también juega un papel clave en el tratamiento y purificación de agua, impactando directamente en nuestra salud y el medioambiente. Al comprender estos procesos, no solo estás aprendiendo química, sino que también estás explorando cómo estos principios se aplican en situaciones cotidianas que afectan nuestras vidas.
Temas Importantes
Disociación
La disociación es un proceso químico donde un compuesto iónico se separa en iones más pequeños al disolverse en agua. Este fenómeno es clave para entender cómo se comportan sustancias como el NaCl (cloruro de sodio) en soluciones acuosas. Cuando el NaCl se agrega al agua, se disocia, liberando iones Na+ y Cl-, esenciales para muchas reacciones químicas, incluyendo la neutralización de ácidos.
-
Los iones resultantes de la disociación pueden conducir electricidad, una propiedad que se utiliza para probar la disociación en el laboratorio.
-
La disociación es crucial en procesos industriales y en el tratamiento del agua, donde el equilibrio iónico necesita ser controlado con cuidado.
-
Entender la disociación ayuda a anticipar el comportamiento de las soluciones en reacciones químicas, especialmente en reacciones de neutralización.
Ionización
La ionización se refiere a la generación de iones a partir de moléculas neutras al disolverse en agua, como sucede con el HCl (ácido clorhídrico). Cuando el HCl se añade al agua, se ioniza formando iones H+ y Cl-. Este proceso es fundamental para entender cómo se comportan los ácidos fuertes en solución, influyendo en todo, desde el pH hasta la reactividad química de la solución.
-
La ionización de los ácidos fuertes es casi completa en solución acuosa, lo que los hace sumamente reactivos.
-
El conocimiento sobre la ionización es vital para entender conceptos como la fuerza de ácidos y bases, así como su comportamiento en reacciones químicas.
-
La ionización es un concepto clave para el desarrollo de estrategias que aborden ácidos y bases en entornos industriales y naturales.
Métodos de Prueba
Los métodos de prueba, como la medición del pH y la conductividad, son esenciales para diferenciar entre disociación e ionización en el laboratorio. Estas pruebas ayudan a determinar la naturaleza iónica de una solución, algo crucial para muchos procesos químicos e industriales. Por ejemplo, evaluar el pH de una solución puede revelar si un ácido se ha ionizado completamente, mientras que la conductividad indica la presencia de iones libres que pueden conducir electricidad.
-
Las mediciones de pH pueden ayudar a identificar la fuerza de un ácido o base según la cantidad de ionización que ocurre.
-
La conductividad se utiliza para verificar la efectividad de la disociación o ionización de una sustancia en solución.
-
Estas pruebas son fundamentales tanto en laboratorios de investigación como en el control de calidad dentro de las industrias.
Términos Clave
-
Disociación: Proceso en el cual un compuesto iónico se separa en iones más pequeños en solución.
-
Ionización: Generación de iones a partir de moléculas neutras al disolverse en agua.
-
pH: Medida de acidez o alcalinidad de una solución, relacionada de manera directa con los procesos de disociación e ionización.
-
Conductividad: Propiedad que indica la capacidad de una solución para conducir electricidad, útil para medir la presencia y concentración de iones.
Para Reflexionar
-
¿Cómo puede ayudar la comprensión de la disociación y la ionización en prácticas sostenibles de tratamiento de agua?
-
¿De qué manera influye el entendimiento de la ionización en la efectividad de los medicamentos que utilizas en tu día a día?
-
¿Cuál es la importancia de medir el pH y la conductividad en industrias que emplean procesos químicos?
Conclusiones Importantes
-
Hoy analizamos las diferencias clave entre disociación e ionización, conceptos fundamentales que impactan todo, desde la purificación del agua hasta la eficacia de los medicamentos.
-
Comprendimos cómo el NaCl se disocia en agua, liberando iones Na+ y Cl-, y cómo el HCl se ioniza para formar iones H+ y Cl-.
-
Discutimos la relevancia de pruebas como el pH y la conductividad para identificar y diferenciar estos procesos químicos en soluciones, algo crucial en muchos campos de la ciencia y la tecnología.
Para Ejercitar el Conocimiento
- Experimento de Disociación e Ionización en Casa: Utiliza sal de mesa (NaCl) y vinagre (ácido acético) para observar la disociación y la ionización. Disuélvelos en agua por separado y observa sus reacciones.
- Diario de Observación Química: Durante una semana, anota todas las reacciones químicas que observes en tu vida diaria, ya sean naturales o inducidas.
- Mapa Conceptual: Crea un mapa conceptual que diferencie disociación e ionización, usando ejemplos del día a día y de la lección.
Desafío
🕵️♂️ Desafío del Detective Químico: Identifica al menos tres productos en tu hogar que sufran disociación o ionización. Explica el proceso químico involucrado y cómo afecta el uso del producto.
Consejos de Estudio
-
Revisa tus notas de la lección y trata de explicar los conceptos de disociación e ionización a un amigo o familiar. ¡Enseñar es una excelente forma de aprender!
-
Mira videos educativos que muestren disociación e ionización en el laboratorio para visualizar mejor los conceptos tratados.
-
Usa juegos educativos y aplicaciones de química para reforzar tu comprensión de las propiedades de las sustancias en solución.