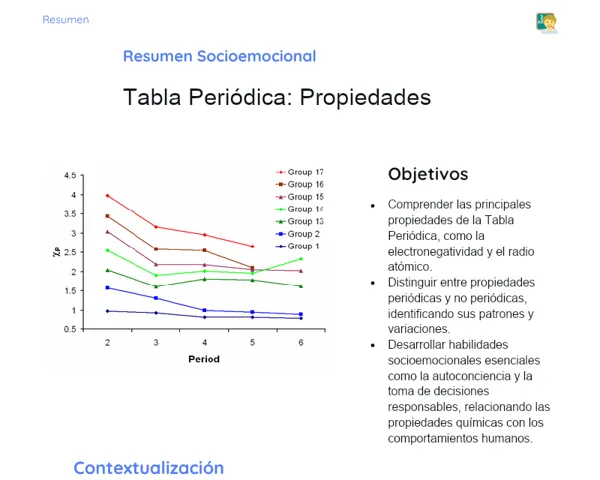
Objetivos
1. 🎯 Comprender los principios fundamentales de la Ley de Proust, que establece que las sustancias compuestas se forman siempre por componentes en proporciones de masa fijas.
2. 🎯 Aplicar la Ley de Proust en diferentes contextos prácticos y teóricos, incluyendo el cálculo y la verificación experimental de proporciones estequiométricas en reacciones químicas.
Contextualización
¿Sabías que la Ley de Proust, también conocida como la Ley de Proporciones Definidas, fue una de las primeras leyes clave de la química moderna y fue formulada por el químico francés Joseph Proust en 1794? Este hallazgo cambió nuestra visión sobre la formación de sustancias químicas y resulta fundamental en muchas aplicaciones prácticas, desde la cocina hasta la seguridad alimentaria y la medicina forense. Dominar estos conceptos no solo te ayudará a destacarte en química, ¡sino también a comprender mejor el mundo que te rodea!
Temas Importantes
Ley de Proporciones Definidas (Ley de Proust)
La Ley de Proust, formulada por el químico francés Joseph Proust, establece que una sustancia química compuesta se forma siempre mediante la combinación de sus elementos en proporciones de masa fijas y definidas. Esto implica que, sin importar la fuente de la sustancia, las proporciones de masa de sus componentes son constantes.
-
Esta ley es esencial para la comprensión básica de la química, ya que permite predecir las cantidades de sustancias formadas o consumidas en una reacción química.
-
Su aplicación es vital en múltiples áreas, incluida la química analítica y ambiental, donde es imprescindible la determinación precisa de compuestos químicos.
-
La Ley de Proust también juega un rol crucial en la industria, especialmente en la producción de productos químicos y farmacéuticos, garantizando la consistencia y calidad de los materiales.
Proporciones Estequiométricas
Las proporciones estequiométricas hacen referencia a las relaciones cuantitativas entre reactivos y productos en una reacción química. Estas proporciones son establecidas por la Ley de Proust y son fundamentales para el cálculo de reacciones químicas, ayudando a predecir la cantidad de productos que se generan o los reactivos necesarios.
-
Entender las proporciones estequiométricas permite a los químicos optimizar la eficiencia de las reacciones, minimizando el desperdicio y maximizando la producción de los productos deseados.
-
Se utilizan en variadas aplicaciones prácticas, como en el diseño de procesos químicos industriales y en la preparación de medicamentos, donde la precisión en las cantidades es crucial para la eficacia del producto final.
-
Estudiar las proporciones estequiométricas también fomenta el desarrollo de habilidades matemáticas aplicadas, ya que con frecuencia implican cálculos y conversiones de unidades.
Aplicaciones de la Ley de Proust
La Ley de Proust no se limita solo al ámbito académico, sino que tiene aplicaciones significativas en diferentes contextos. Desde la cocina, donde la precisión en las proporciones de los ingredientes es fundamental para lograr una buena receta, hasta la medicina forense, donde el análisis de sustancias puede ayudar a esclarecer causas de muerte, la Ley de Proust se vuelve indispensable.
-
En la cocina, comprender las proporciones correctas de los ingredientes asegura que los platos tengan la calidad y consistencia esperadas.
-
En el ámbito forense, el análisis de sustancias en muestras biológicas se basa en la Ley de Proust para detectar drogas o venenos, lo cual es crucial en investigaciones criminales.
-
La Ley de Proust también tiene aplicaciones en la fabricación de materiales y el desarrollo de nuevas tecnologías, donde se requiere precisión y fiabilidad en los procesos.
Términos Clave
-
Ley de Proust: Establece que una sustancia química compuesta siempre se forma por la combinación de sus componentes en proporciones de masa fijas.
-
Proporciones Estequiométricas: Relaciones cuantitativas entre reactivos y productos en una reacción química, determinadas por la Ley de Proust.
-
Compuesto Químico: Una sustancia formada por la combinación de elementos en proporciones fijas, de acuerdo con la Ley de Proust.
Para Reflexionar
-
¿Cómo puede el entendimiento de las proporciones estequiométricas contribuir a reducir el desperdicio y aumentar la eficiencia en los procesos industriales?
-
¿De qué maneras la aplicación de la Ley de Proust en contextos diversos, como la cocina y la medicina forense, demuestra la universalidad de los principios químicos?
-
¿Cuál es la importancia de aprender sobre las leyes fundamentales de la química, como la Ley de Proust, más allá de las aplicaciones académicas en el mundo actual?
Conclusiones Importantes
-
Revisamos la Ley de Proust y cómo establece las bases para entender que las sustancias compuestas se forman por elementos en proporciones de masa fijas.
-
Discutimos la aplicación práctica de la Ley de Proust en diversas áreas, desde la cocina hasta la medicina forense, resaltando la relevancia de estos conceptos químicos en situaciones cotidianas y en otros campos.
-
Exploramos cómo las proporciones estequiométricas son esenciales para predecir y controlar reacciones químicas, siendo clave para aplicaciones industriales, científicas y tecnológicas.
Para Ejercitar el Conocimiento
- Prepará una receta de pastel pero, en lugar de seguir la receta al pie de la letra, intentá ajustar las proporciones de los ingredientes y observá cómo influye en el resultado final. 2. Realizá un pequeño experimento en casa o en la escuela mezclando vinagre y bicarbonato de sodio en diferentes proporciones, midiendo la cantidad de gas liberado para verificar la Ley de Proust. 3. Elegí un producto químico de uso doméstico e investigá sus ingredientes. Intenta predecir las proporciones posibles de los elementos según su función y la Ley de Proust.
Desafío
Desafío del Detective Químico: Creá un escenario criminal en el que se haya utilizado un veneno. Basándote en las pistas químicas encontradas, como proporciones de elementos en muestras biológicas, identifica el veneno utilizando la Ley de Proust y otras leyes químicas que hemos aprendido.
Consejos de Estudio
-
Revisá regularmente las proporciones estequiométricas, practicando con ejemplos variados para fortalecer tu comprensión de los conceptos.
-
Mirate videos educativos que demuestren la aplicación práctica de la Ley de Proust en diferentes campos, para visualizar el concepto en acción.
-
Formá grupos de estudio para discutir y resolver problemas relacionados con las leyes de peso, compartiendo diferentes perspectivas y estrategias de resolución de problemas.